|
今日、学校で、ペンキ塗りがありました。
初めて塗りました。
服が汚れたけど、楽しかったです。
(PS)
この前書いた、電気分解の話について書きます。
普通、原子は下の図のように、電子の通る道があります。

中にある、+が、原子核です。
そして、その外側が、Kかくです。
一番外側にあるのが、Lかくです。
Lかくの外にも、MNOPQRといっぱいあります。
Kかくは、2個電子が入ります。
Lかくは、8個電子が入ります。
原子は、一つずつ電子が増えるので、10個の原子が作れます。
今回は、水の電気分解なので、水素と酸素の絵を書きました。
下の図は水素です。
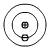
水素は、電子がひとつです。
Kかくに、電子が一つ入っています。
だから、もう一個電子が無いと、Kかくが安定しません。
次に酸素です。
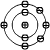
これは、電子が8つあります。
Kかくに2つ、Lかくに、6つ電子があります。
あと二個電子を足さないと、Lかくが、つりあいません。
水素二つに、酸素一つでつりあいますね。
よく考えてみると、これで、水(H2O)が出来ます。
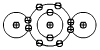
これは水のモデルです。
ちゃんとつりあっています。
では、これを分解してみましょう。
電気が加わると、酸素と水素が分かれます。
そのときに、酸素はつりあっていません。
どうすればつりあうでしょうか?
ひとつは、電子を全てなくすのです。
もうひとつは、電子を二つ足します。
どちらのほうがエネルギーが少ないでしょうか?
そうです。
電子を、8つ取るよりも、2つ足したほうがいいですね。
そしたら、どこから電子を取りましょうか?
それは、水素からです。
水素は、足してもひいても1なので、今回は電子をなくすのです。
すると、酸素と水素は、両方ともつりあいます。
でも、酸素はマイナスが増え、マイナスイオンになります。
すると、プラスの電極に引寄せられます。
一方水素は、マイナスが足りないので、プラスイオンになります。
だから、マイナスの電極に引寄せられます。
酸素は、電極についたら、電気を水素に渡します。 |
|

